Новый подход к борьбе с курением: психофизиологический анализ
Поступила: 19.12.2013
Принята к публикации: 26.12.2013
Страницы: 91-99
DOI: 10.11621/npj.2013.0212
Ключевые слова: теория поэтапного формированиявысших психических функций Гальперина; курение; отказ от курения по методу Захарова; мозг; электроэнцефалограмма; вегетативная нервная система
Захаров В.М., Королев А.Д., Черноризов А.М. (2013). Новый подход к борьбе с курением: психофизиологический анализ. Национальный психологический журнал, (1) , 91-99. https://doi.org/10.11621/npj.2013.0212
Скопировано в буфер обмена
СкопироватьАннотация
В статье излагаются результаты пилотного психофизиологического исследования изменений активности мозга и вегетативной нервной системы (ВНС) человека, бросающего курить табак по методу, предложенному отечественным исследователем В.М. Захаровым. Метод базируется на теории поэтапного формирования высших психических функций П.Я. Гальперина.
В экспериментах приняли участие 16 человек (8 мужчин и 8 женщин). Анализировался спектральный состав электроэнцефалограммы (ЭЭГ), где в расчет принимались абсолютные значения мощностей альфа-ритма (в отведениях O2-A2, O1-A1, P4-A2, P-A1) и бета-ритма (в отведениях F4-A2, F3-A1). Активность вегетативной нервной системы (ВНС) оценивалась по результатам анализа электрокардиограммы (ЭКГ). Данные о субъективной оценке испытуемыми своего наличного функционального состояния получались посредством их психологического тестирования по методике «Самочувствие. Активность. Настроение» (САН). По результатам пилотного исследования было установлено, что функциональное состояния нервной системы (оценки по параметрам ЭЭГ и ЭКГ) и субъективное (психологическое) состояния (оценки по данным САН) человека во время курения и попытки бросить курить зависят не только от стажа потребления табака, но и от отношения курящего к процессу табакокурения. Когнитивная активность хронического курильщика в процессе курения (осуществление контроля количества выкуриваемого табака) как бы возвращает его в исходное до формирования зависимости от табака состояние «некурящего» и тем самым облегчает ему решение задачи «бросить курить». Полученные данные носят предварительный характер и требуют дальнейшего уточнения. В перспективе они могут быть использованы при разработке «психологических стратегий» для помощи курящему в его борьбе с зависимостью от табака.
За рубежом наибольшей популярностью пользуются стратегии борьбы с курением, основанные на применении фармакологических препаратов (Fant et al., 2009), использовании электронных сигарет и сигарет с пониженным содержанием никотина (Benowitz, 2009), индивидуальных пошаговых планов-графиков отказа от курения (Сайт проекта «Никвитин», 2014). Каждая из этих стратегий в чем-то «проигрывает» конкурентным альтернативам, так как ориентирована на отдельные специфические аспекты табачной аддикции – биохимические, физиологические или же поведенческие.
Особенность предложенного отечественным исследователем В.М. Захаровым (Захаров, 2011, 2012) метода борьбы с этой вредной привычкой состоит в том, что он базируется на достижениях современной психологии, а именно, на теории поэтапного формирования высших психических функций, разработанной выдающимся отечественным психологом П.Я. Гальпериным (1976). Этот метод предполагает постепенное прекращение курения с применением специально разработанной для этой цели процедуры. На курительную часть сигареты наносились круговые метки в виде полосок, которые делили ее на три равные части, соответствующие дозам выкуриваемого табака.
Курильщику предлагалось не просто курить сигарету, а с помощью этих рисок контролировать количество выкуриваемого табака. Предполагалось, что метки на сигаретах, постоянно находясь в поле зрения курильщика, будут стимулировать процесс «когнитивного контроля» над количеством выкуриваемого табака, постепенно (поэтапно) ослабляя своего «эмоционального оппонента» – удовольствие от процесса курения. Благодаря этому, курильщик избавляется от вредной привычки в щадящем режиме, не порывая с курением моментально. Важно отметить, что при использовании метода визуального контроля над количеством выкуриваемого табака курильщику для достижения успеха не требуется слишком высокий уровень мотивации (Захаров, 2011).
Реализация этого метода на тысячах человек продемонстрировала его высокую эффективность (Захаров, 2011, 2012). Возникают вопросы, касающиеся психофизиологических механизмов такой эффективности:
меняется ли и, если «да», то «как» и «где» паттерн активности мозга в процессе отказа то курения по «методу Захарова»;
о чем свидетельствуют эти изменения?
В настоящей статье излагаются результаты пилотного психофизиологического исследования, посвященного поиску ответов на эти вопросы.
Проведение исследования
Психофизиологический эксперимент
В соответствии с рекомендациями Комиссии по биомедицинской этике при МГУ имени М.В. Ломоносова, все испытуемые дали письменное согласие на участие в экспериментах.
В психофизиологическом исследовании приняли участие 16 человек – 8 мужчин и 8 женщин. Участники исследования были распределены на 4 непересекающиеся группы (2 мужчин и 2 женщин в каждой группе).
В первую группу вошли испытуемые, которые никогда не курили табак и добровольно согласились выкурить сигарету в эксперименте. Инструкция членам этой группы: во время психофизиологического эксперимента просто курить сигарету.
Во вторую группу вошли испытуемые, которые регулярно курят табак, но, по условию эксперимента, не курили, как минимум, в течение суток до начала испытаний. Инструкция членам этой группы: во время психофизиологического эксперимента просто курить сигарету.
В третью группу были включены испытуемые, которые регулярно курят табак и, по данным их самоотчетов, курение никогда не прерывали. Инструкция членам этой группы: во время психофизиологического эксперимента просто курить сигарету.
В четвертую группу вошли участники эксперимента, которые регулярно курили. Им, в отличие от членов первых трех групп, была дана другая инструкция: во время эксперимента не просто курить сигарету, а контролировать количество выкуриваемого табака с помощью заранее нанесенных на сигарете рисунков.
Группы 1-3 выполняли функцию контрольных групп, а группа 4 была экспериментальной группой.
Эксперимент, заключающийся в регистрации ряда физиологических показателей (описание см. ниже п. 2.3) до, во время и после курения, длился 25-30 мин и включал 5 последовательно реализуемых функциональных проб (ФП):
ФП 1: испытуемый сидит в кресле в удобном положении, при этом глаза открыты (0-300 с);
ФП 2: испытуемый сидит в кресле, его глаза закрыты (300-600 с);
ФП 3: испытуемый выкуривает сигарету согласно инструкции (600-720 (900) с);
ФП 4: испытуемый сидит в кресле с закрытыми глазами (720 (900)-1020 (1200) с);
ФП 5: испытуемый сидит в кресле с открытыми глазами (1020 (1200)-1320 (1500) с).
Регистрация физиологических реакций во время эксперимента производилась с помощью программно-аппаратного комплекса «Энцефалан 131-03».
Электроэнцефалограмма (ЭЭГ) регистрировалась в 21 отведении: Fp1, Fpz, Fp2, F7, F3, Fz, F4, F8, T3, C3, Cz, C4, T4, T5, P3, Pz, P4, T6, O1, Oz, O2 – по международной системе 10-20 (Jasper, 1958). Схема отведения – базовая монополярная. Два референтных электрода (A1, A2) фиксировались на мочках ушей. Частота дискретизации записи – 250 Гц. Фильтр низких частот (ФНЧ) – 70 Гц, фильтр высоких частот (ФВЧ) – 0,16 Гц, режекция сетевой помехи – 50 Гц. Сопротивление под электродами не превышало 15 кОм. Для снижения сопротивления между кожей головы и электродами использовался высокопроводящий гель «Унимакс». После записи ЭЭГ производилась ее первичная обработка – удалялись артефакты от движений глаз, рук и головы. После первичной обработки записи ЭЭГ обрабатывались и анализировались с помощью программного обеспечения, разработанного «НПК Медиком-Мтд». Для обработки ЭЭГ применялся спектральный анализ (Гнездицкий, 1997, 2000). Спектр мощности, получаемый в результате спектрального анализа, отражал энергию каждой из частотной составляющих выбранного фрагмента ЭЭГ в каждом отведении и позволял проанализировать степень выраженности и характер пространственного распределения выделенных частот по поверхности головы.
Спектры мощности (спектрограммы) позволили оценить значения частот наиболее выраженных компонентов, как по доминирующему ритму, так и по менее выраженным ритмам. По степени «размазанности» основных пиков ритма можно было оценить его регулярность по частоте. Сравнением амплитуд пиков и значений соответствующих им частот на спектрограммах симметричных отведений можно было выявить наличие мощностной или частотной асимметрии. Мощностной спектр используется чаще, чем амплитудный, потому что он более нагляден, и на нем лучше видны имеющиеся фокальные патологические очаги. В программном пакете к комплексу «Энцефалан-131-03» (МЕДИКОМ-МТД, 2006) для вычисления спектральных характеристик энцефалографического сигнала используется дискретное преобразование Фурье (ДПФ). ДПФ представляет собой математическую процедуру преобразования данных из временной области в частотную.
Данный метод известен как метод периодограмм, а его частные реализации, основанные на усреднении по ансамблям, известны как «периодограммы Бартлетта и Уэлча» (Гнездицкий, 1997, 2000). По результатам спектрального анализа производился расчет мощностей альфа-ритма (8-13 Гц), бета-ритма (13-35Гц). Увеличение мощности альфа- ритма свидетельствовало о понижении уровня активации мозга, а увеличение мощности бета-ритма – о повышении уровня активации в ситуациях физического, эмоционального или интеллектуального напряжения. При анализе полученных результатов в расчет брались абсолютные значения мощностей альфа- и бета-ритмов, полученные со следующих отведений ЭЭГ:
|
Альфа-ритм (8-13 Гц) |
O2-A2 O1-A1 P4-A2 P3--A1 |
|
Бета-ритм (13-35 Гц) |
F4-A2 F3-A1 |
Запись ЭЭГ испытуемого до, во время и после эксперимента осуществлялась в двух стандартных для электроэнцефалографии функциональных пробах – с закрытыми глазами (ФЗГ) и с открытыми глазами (ФОГ). Ситуация ФЗГ является оптимальной для регистрации альфа-ритма, а ситуация ФОГ – для регистрации высокочастотных бета-колебаний.
Запись электрокардиограммы (ЭКГ) производилась с помощью двух электродов, закрепленных на предплечьях испытуемых. Заземление канала производилось за счет постановки дополнительного электрода на левое предплечье; ФНЧ – 30Гц, ФВЧ – 0,5Гц. По результатам стандартизированного математического анализа ЭКГ (Баевский и др., 1996) производился расчет следующих показателей сердечнососудистой деятельности, активности симпатического и парасимпатического отделов вегетативной нервной системы (ВНС):
частота сердечных сокращений (ЧСС). Увеличение (уменьшение) ЧСС отражает увеличение (уменьшение) активности сердца;
распределение RR-интервалов (RR). Увеличение значений показателя RR свидетельствует об усилении модулирующего влияния на сердце парасимпатического отдела ВНС, уменьшение – о подключении к модуляции симпатического отдела ВНС;
мощность спектра высокочастотного компонента вариабельности сердечного ритма в процентах от суммарной мощности колебаний (HF, %,). Этот индикатор, рассчитываемый с помощью спектрального анализа ЭКГ, отражает относительный уровень активности парасимпатического звена регуляции сердечной деятельности;
мощность спектра низкочастотного компонента вариабельности сердечного ритма в процентах от суммарной мощности колебаний (LF, %). Этот индикатор, рассчитываемый с помощью спектрального анализа ЭКГ, отражает относительный уровень активности симпатического звена регуляции сердечной деятельности;
отношение значений низкочастотного и высокочастотного компонентов вариабельности сердечного ритма (LF/HF). Увеличение значения показателя свидетельствует об усилении влияния симпатического отдела (ослаблении влияния парасимпатического отдела), а уменьшение – об усилении влияния парасимпатического отдела (ослаблении влияния симпатического отдела).
По дополнительному каналу комплекса «Энцефалан-131-03» производилась регистрация фотоплетизмограммы (ФПГ), датчик которой располагался на среднем пальце левой руки испытуемого. Для целей исследования использовались значения амплитуды систолической волны (АСВ), получаемые в результате спектрального анализа ФПГ. Увеличение значений АСВ свидетельствует об усилении модулирующего влияния на периферические сосуды парасимпатического отдела, а уменьшение – симпатического отдела ВНС (Захаров, Скоморохов, 2012).
Психологическое тестирование
До и после проведения психофизиологического эксперимента испытуемым предлагалось заполнить психологический опросник «САН» (Самочувствие. Активность. Настроение). Тест «САН» — разновидность опросников состояний и настроений, разработанный сотрудниками 1-го Московского медицинского института имени И.М. Сеченова (Доскин и др., 1973). Этот бланковый тест предназначен для оперативной оценки испытуемым своего наличного функционального состояния по семибалльной шкале со значениями от 1 (крайне плохое самочувствие и низкая активность, очень плохое настроение) до 7 (очень хорошее самочувствие, высокий уровень бодрствования, прекрасное настроение). Следует упомянуть, что при анализе функционального состояния важны не только значения отдельных его показателей, но и их соотношение. Так, у отдохнувшего человека оценки активности, настроения и самочувствия примерно равны (Доскин и др., 1973). А по мере нарастания усталости соотношение между ними изменяется за счет относительного снижения самочувствия и активности по сравнению с настроением.
В итоге, вся экспериментальная процедура – заполнение «САН» и психофизиологический эксперимент с выкуриванием сигареты занимала 45-50 мин.
Результаты исследования
Описываемые ниже данные представляют результаты пилотного исследования, используемые для выявления «тенденций» и не предназначенные для полноценного статистического анализа.
Результаты психологического тестирования испытуемых всех четырех групп с помощью опросника «САН» сведены в таблицу 3.1.
|
«Ник» испытуемого |
Оценка до исследования |
Оценка после исследования |
«Сумма всех баллов после исследования» - «Сумма всех баллов до исследования» (в % от суммы до исследования) |
||||
|
|
С |
А |
Н |
С |
А |
Н |
|
|
Первая группа испытуемых |
|||||||
|
В.Р. |
6,3 |
6,2 |
6,7 |
2,9 |
4,7 |
3,9 |
-7,7 (-40%) |
|
Б.С. |
5,5 |
4,7 |
5,7 |
4,7 |
3,1 |
4,6 |
-3,5 (-22%) |
|
К.Е. |
2,9 |
5,5 |
1,5 |
5,5 |
6,5 |
5,2 |
7,3 (73%) |
|
Л.В. |
5,3 |
5,8 |
5,7 |
4,4 |
3,7 |
5,3 |
-3,4 (-20,2%) |
|
Вторая группа испытуемых |
|||||||
|
К.П. |
5,1 |
4,2 |
5,2 |
5,2 |
4,0 |
5,4 |
0,1 (0,7 %) |
|
Е.В. |
4,8 |
5,1 |
5,1 |
6,0 |
6,0 |
6,0 |
3,0 (20 %) |
|
Ак.Е. |
5,7 |
4,6 |
5,8 |
5,7 |
5,0 |
5,8 |
0,4 (2,5 %) |
|
Ан.Е. |
6,0 |
3,6 |
6,4 |
6,4 |
3,4 |
6,8 |
0, 6 (3,8 %) |
|
Третья группа испытуемых |
|||||||
|
П.А. |
3,7 |
4,3 |
3,7 |
3,7 |
4,0 |
3,7 |
- 0,3 (- 2,6 %) |
|
Н.Л. |
5,3 |
5,2 |
4,5 |
4,7 |
4,9 |
4,0 |
- 1,4 (- 9,3 %) |
|
А.Е. |
3,0 |
3,9 |
2,6 |
4,1 |
3,8 |
4,5 |
2,9 (30,5 %) |
|
З.М. |
5,5 |
5,4 |
6,6 |
6,0 |
4,9 |
6,6 |
0 (0 %) |
|
Четвертая группа испытуемых |
|||||||
|
К.А. |
4,9 |
5,1 |
6,0 |
4,9 |
5,8 |
5,6 |
0,3 (10 %) |
|
М.В. |
4,3 |
4,1 |
6,5 |
3,8 |
2,3 |
6,4 |
- 2,4 (-16,1 %) |
|
Щ.И. |
5,9 |
5,4 |
5,5 |
5,6 |
5,1 |
5,8 |
- 0,3 (- 1,8 %) |
|
П.Н. |
6,1 |
6,5 |
6,8 |
6,4 |
6,5 |
5,6 |
- 0,9 (- 4,6 %) |
Таблица 3.1. Результаты тестирования испытуемых всех четырех групп с использованием опросника «САН»
Из таблицы 3.1 видно, что у трех впервые закуривших испытуемых первой группы наблюдается ухудшение самочувствия, активности и настроения, что закономерно для начинающих курильщиков. Исключение – испытуемая К.Е., отличавшаяся от других членов группы исходно (до исследования) низкими самооценками самочувствия и настроения, которые резко (в 2-3 раза) увеличились после выкуривания сигареты. Исходно высокий балл по шкале «активность» (5.5) у этой испытуемой после курения увеличился незначительно (6.5).
Для второй группы испытуемых, как видно из таблицы, небольшой (24 час) перерыв в курении приводит в среднем к незначительному увеличению показателей «САН» – улучшению самочувствия, повышению активности и настроения.
В третьей группе испытуемых со стажем курения 2-3 года после курения наблюдаются небольшие колебания в силе и направлении изменений показателей «САН». Однако, у испытуемого П.А. с большим стажем курения (10 лет) одна выкуренная сигарета мало сказалась на показателях теста, что ожидаемым образом свидетельствует о выраженности эффекта привыкания.
Для испытуемых четвертой, контрольной группы показатели наличного функционального состояния по тесту – самооценки самочувствия, активности и настроения в результате курения с контролем над выкуриваемой дозой табака меняются индивидуально, но в целом (по сумме оценок «САН») с тенденцией к небольшому ухудшению состояния.
О характере изменений ритмической активности мозга каждого испытуемого из четырех групп после эксперимента с курением относительно ритмической активности до эксперимента можно судить по данным таблицы 3.2.
Примечания:
обозначения и частотные диапазоны ритмов см. п. 2.3.1;
направление стрелок обозначает уменьшение (стрелка вниз) или же увеличение (стрелка вверх) мощности того или иного ритма ЭЭГ в ФП 4-5 (после эксперимента) относительно мощности ритма в ФП 1-2 (до эксперимента);
цифрами указаны величины изменений мощности ритмов в ФП 4-5 в процентах от мощности ритмов в ФП 1-2. Например «ФОГ -0,7» в столбце» «Альфа-ритм» означает, что мощность альфа-ритма в пробе «закрытые глаза ПОСЛЕ курения» (ФП 4) выросла по отношению к мощности этого ритма в пробе «закрытые глаза ДО курения» (ФП 2) на 0,7 %.
|
Группы |
Пол |
«НИК» испыт. |
Альфа-ритм |
Бета-ритм |
||
|
ФОГ |
ФЗГ |
ФОГ |
ФЗГ |
|||
|
Никогда не курили. Выкурили свою первую сигарету в эксперименте. |
М |
В. Р. |
32,5 |
0,7 |
34,9 |
15,2 |
|
М |
Б. С. |
16,3 |
7,6 |
15,9 |
14,3 |
|
|
Ж |
К. Е. |
18,2 |
32,2 |
20,2 |
5 |
|
|
Ж |
Л. В. |
0,4 |
33 |
20,5 |
13,3 |
|
|
Не курили 24 часа до начала эксперимента. Первую сигарету после перерыва выкурили в эксперименте. |
М |
К. П. |
5,1 |
5,5 |
16,7 |
34,8 |
|
М |
Е. В. |
62,8 |
8,1 |
8,8 |
27,2 |
|
|
Ж |
Ак. Е. |
30,5 |
62,1 |
1,7 |
9,8 |
|
|
Ж |
Ан. Е. |
13,9 |
56,3 |
17,6 |
2,1 |
|
|
За весь свой стаж курения не делали перерывов в табакокурении. И в том числе, выкурили сигарету на эксперименте. |
М |
П. А. |
35 |
53,1 |
19,4 |
38,5 |
|
М |
Н. Л. |
15,1 |
38,6 |
36,3 |
19,9 |
|
|
Ж |
А. Е. |
16,9 |
24,6 |
29 |
1,3 |
|
|
Ж |
З. М. |
49,2 |
54,7 |
0,6 |
6,1 |
|
|
За весь свой стаж курения не делали перерывов в табакокурении. Выкурили сигарету в эксперименте, контролируя количество выкуриваемого табака. |
М |
К. А. |
11,9 |
33 |
17,8 |
14,2 |
|
М |
М. В. |
29,9 |
1,1 |
14 |
10,4 |
|
|
Ж |
П. Н. |
7,1 |
69,1 |
3,9 |
6,2 |
|
|
Ж |
Щ. И. |
17,1 |
22,6 |
50,7 |
77,5 | |
Таблица 3.2. Динамика (направление и величина) изменений мощности ритмов ЭЭГ после эксперимента с курением в ФП 4 (ФОГ, фоновая ЭЭГ с открытыми глазами) и ФП 5 (ФЗГ, фоновая ЭЭГ с закрытыми глазами) относительно мощности этих же ритмов до эксперимента в ФП 1-2
Из таблицы 3.2 видно, что изменения выраженности в ЭЭГ альфа-ритма (8-13 Гц) в результате курения у всех испытуемых первой группы, за небольшим исключением, носили однонаправленный характер: мощность этого ритма в среднем уменьшилась в ФП 4 («закрытые глаза», ФЗГ) на 18%, а в ФП 5 («открытые глаза», ФОГ) – на 8%. Активность же мозга в диапазоне бета-колебаний менялась прямо противоположным образом в зависимости от фактора «открытые глаза/ закрытые глаза» : при открытых глазах (ФОГ) мощность бета-ритма уменьшалась после курения, в среднем, на 23 %, а при закрытых глазах (ФЗГ) – увеличилась на 12% (таблица 3.2). Здесь мы фиксируем некоторый парадокс. Согласно данным классической нейрофизиологии, уменьшение мощности альфа-ритма («реакция депрессии альфа-ритма»), отражает повышение активности мозга и сопровождается увеличением представленности в ЭЭГ высокочастотных бета- и гамма- ритмов. Мы же наблюдаем факт сопряжения понижения выраженности альфа-ритма в ФЗГ и в ФОГ с разнонаправленным изменением мощности бета-ритма: повышением выраженности бета-колебаний в ФЗГ и снижением – в ФОГ.
У испытуемых второй группы, за небольшими исключениями, данные таблицы 3.2 свидетельствуют об увеличении активности мозга после курения.
Для испытуемых третьей группы данные таблицы свидетельствуют о том, что после курения (в ситуациях как ФОГ, так и ФЗГ) наблюдается синхронное уменьшение мощности альфа- и бета-ритмов.
Из анализа данных таблицы 3.2 следует, что у испытуемых четвертой группы К.А. и М.В. увеличение мощности альфа-ритма сопровождается одновременным повышением выраженности в ЭЭГ бета-ритма, а у испытуемых П.Н. и Щ.И. уменьшение мощности альфа-ритма сопряжено, за одним исключением, с повышением мощности бета-ритма. Таким образом, в целом по группе мощность бета-ритма во всех ФП увеличивается при разнонаправленном изменении альфа-ритма.
Изменения сердечнососудистой деятельности организма каждого испытуемого из первой группы после эксперимента с курением представлены показателями ЭКГ и ФПГ в таблице 3.3.
Примечание: Обозначения те же, что и к таблицам 3.2.
|
Группы |
Пол |
«НИК» испыт. |
ЧСС |
RR |
АСВ |
LF/HF |
||||
|
ФОГ |
ФЗГ |
ФОГ |
ФЗГ |
ФОГ |
ФЗГ |
ФОГ |
ФЗГ |
|||
|
Никогда не курили. Выкурили свою первую сигарету в эксперименте. |
М |
В. Р. |
47,7 |
12,7 |
5,9 |
11,5 |
48,2 |
13,7 |
7,1 |
45,2 |
|
М |
Б. С. |
5,2 |
5,1 |
4,7 |
4,7 |
14 |
2,7 |
35,4 |
45,9 |
|
|
Ж |
К. Е. |
6,7 |
1,6 |
5,8 |
2,2 |
59,4 |
47,8 |
17,3 |
2,8 |
|
|
Ж |
Л. В. |
1,4 |
5,3 |
1,8 |
4,9 |
38,6 |
27,9 |
10,3 |
31,9 |
|
|
Не курили 24 часа до начала эксперимента. Первую сигарету после перерыва выкурили в эксперименте. |
М |
К. П. |
11,1 |
32,9 |
18,5 |
25,2 |
43,7 |
48,3 |
87,4 |
249,4 |
|
М |
Е. В. |
5,1 |
11,2 |
5,1 |
10,6 |
45,5 |
50,2 |
38,5 |
93,5 |
|
|
Ж |
Ак. Е. |
22 |
23,5 |
18,2 |
18,8 |
19,1 |
33,3 |
110,9 |
67,6 |
|
|
Ж |
Ан. Е. |
29,6 |
32,9 |
23,6 |
25 |
76 |
51,2 |
377,8 |
92,9 |
|
|
За весь свой стаж курения не делали перерывов в табакокурении. И в том числе, выкурили сигарету на эксперименте. |
М |
П. А. |
16,3 |
20,5 |
13,7 |
16,9 |
91,3 |
93 |
29,8 |
170,1 |
|
М |
Н. Л. |
8,3 |
11 |
7,7 |
10,5 |
53,1 |
36,6 |
8,8 |
31,1 |
|
|
Ж |
А. Е. |
22,7 |
29,7 |
15,8 |
22,2 |
68 |
75 |
67 |
248,6 |
|
|
Ж |
З. М. |
5,1 |
11,2 |
5,1 |
10,6 |
45,5 |
50,2 |
39,9 |
101,7 |
|
|
За весь свой стаж курения не делали перерывов в табакокурении. Выкурили сигарету в эксперименте, контролируя количество выкуриваемого табака. |
М |
К. А. |
6,8 |
6,6 |
7 |
6,4 |
46,7 |
30,8 |
42,3 |
47,5 |
|
М |
М. В. |
8,9 |
13,2 |
8,5 |
11,2 |
58,2 |
45,2 |
33,8 |
36,5 |
|
|
Ж |
П. Н. |
7,77 |
25,8 |
7,4 |
20,7 |
58,5 |
64,3 |
43,1 |
165,3 |
|
|
Ж |
Щ. И. |
13,8 |
22,8 |
11,9 |
18,4 |
59,8 |
80,9 |
216,9 |
913,8 | |
Таблица 3.3. Динамика (направление и величина) изменений показателей ЧСС, RR, ACB, LF/HF и АСВ, зарегистрированных после эксперимента с курением в ФП 4 (ФОГ) и ФП 5 (ФЗГ), относительно значений этих же показателей, зарегистрированных до эксперимента в ФП 1-2
Из таблицы 3.3 следует, что у испытуемых первой группы В.Р., Б.С. и К.Е. после курения большая часть физиологических показателей активности ВНС (ЧСС, RR, АСВ) изменяется по симпатикотропному типу, за исключением показателя LF/HF, обнаруживающего заметные индивидуальные вариации. У испытуемой Л.В. все показатели, за одним исключением (АСВ), демонстрируют парасимпатический паттерн реакций.
Судя по данным таблицы 3.3, практически у всех испытуемых второй, третьей и четвертой групп после курения показатели активности ВНС изменяются при доминировании симпатикотропного отдела, свидетельствуя о повышении общего уровня бодрствования испытуемых после выкуривания сигареты.
Значения физиологических показателей, рассчитанных по данным психофизиологического эксперимента во время курения, приведены в таблице 3.4.
Примечание: Обозначения те же, что и к таблицам 3.2 и 3.3.
|
Группы |
Пол |
«НИК» испыт. |
Альфа- ритм |
Бета- ритм |
ЧСС |
RR |
АСВ |
LF/ HF |
|
Курение (ФП 3) |
||||||||
|
Никогда не курили. Выкурили свою первую сигарету в эксперименте. |
М |
В. Р. |
28,8 |
189,2 |
9,3 |
6,1 |
60,6 |
72,2 |
|
М |
Б. С. |
20,3 |
105,1 |
15,6 |
11,4 |
15,7 |
77,9 |
|
|
Ж |
К. Е. |
48,7 |
52,1 |
10 |
9,3 |
51,9 |
37,8 |
|
|
Ж |
Л. В. |
20,9 |
68,7 |
8,2 |
4,5 |
46,7 |
34,9 |
|
|
Не курили 24 часа. Первую сигарету после перерыва выкурили в эксперименте. |
М |
К. П. |
19,3 |
37,7 |
25 |
19,1 |
55,2 |
435,1 |
|
М |
Е. В. |
52,9 |
20,4 |
5,1 |
5,1 |
42 |
5,6 |
|
|
Ж |
Ак. Е. |
47 |
13,8 |
18,3 |
11,2 |
50,4 |
66,7 |
|
|
Ж |
Ан. Е. |
39,1 |
43,4 |
45,1 |
29,7 |
75,1 |
29,6 |
|
|
За весь свой стаж курения не делали перерывов в табакокурении. И в том числе, выкурили сигарету на эксперименте. |
М |
П. А. |
25 |
33,1 |
12,5 |
10,7 |
83,3 |
168,6 |
|
М |
Н. Л. |
19,2 |
24,5 |
13,9 |
11,7 |
44,6 |
43,6 |
|
|
Ж |
А. Е. |
72,5 |
31 |
28 |
19,5 |
77,9 |
155,4 |
|
|
Ж |
З. М. |
66,6 |
3,9 |
5,1 |
5,1 |
42 |
8,7 |
|
|
За весь свой стаж курения не делали перерывов в табакокурении. Выкурили сигарету в эксперименте, контролируя количество выкуриваемого табака. |
М |
К. А. |
31,3 |
70,7 |
12,2 |
10,8 |
68,7 |
40,7 |
|
М |
М. В. |
31,2 |
47,8 |
12,2 |
11 |
45,4 |
26,4 |
|
|
Ж |
П. Н. |
39 |
59,3 |
23,1 |
21,3 |
22 |
7,3 |
|
|
Ж |
Щ. И. |
5,3 |
342,1 |
21,3 |
16,8 |
74 |
57 | |
Таблица 3.4. Динамика (направление и величина) изменений показателей мощности альфа- и бета- ритмов мозга, ЧСС, RR, ACB, LF/HF и АСВ, зарегистрированных во время эксперимента с курением в ФП 3 (ФОГ), относительно значений этих же показателей, зарегистрированных до эксперимента в ФП 1
Все испытуемые первой группы во время курения обнаружили одинаковый характер изменений в активности мозга (ЭЭГ) и сердечнососудистой деятельности (ЭКГ, ФПГ). Рисунки 3.1-3.6, на которых для примера представлены данные испытуемого В.Р., иллюстрируют типичный для группы паттерн таких изменений.
в ФП 1 с открытыми глазами до выкуривания сигареты (ОГ до курения);
в ФП 2 с закрытыми глазами до курения (ФЗГ до курения);
в ФП 3, когда испытуемый выкуривает сигарету (курение);
в ФП 4 с закрытыми глазами после курения (ФЗГ после курения);
в ФП 5 с открытыми глазами после курения (ОГ после курения).
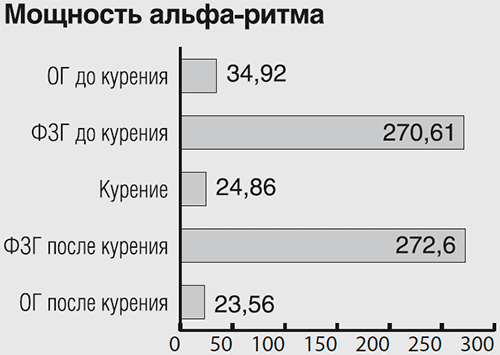
Рисунок 3.1 Значения мощности альфа-ритма ЭЭГ в теменно-затылочных отделах головного мозга (ГМ) (отведения P-P4, O1-O2) испытуемого В.Р. во всех функциональных пробах (ФП):
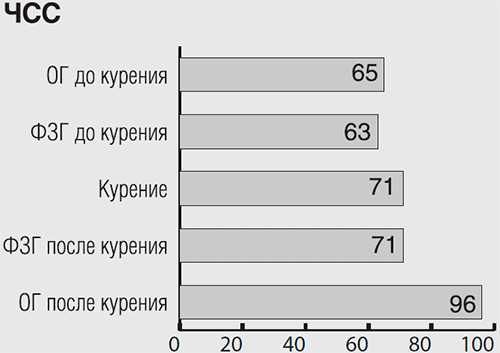
Рисунок 3.2 Значения мощности бета-ритма ЭЭГ в области фронтальных отделов ГМ испытуемого В.Р. (отведения F3-F4) во всех функциональных пробах. Обозначения те же, что и к рисунку 3.1.
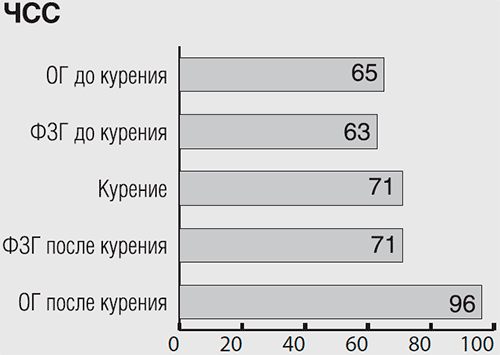
Рисунок 3.3 Значения частоты сердечных сокращений (ЧСС) у испытуемого В.Р. во всех функциональных пробах. Обозначения те же, что и к рисунку 3.1.
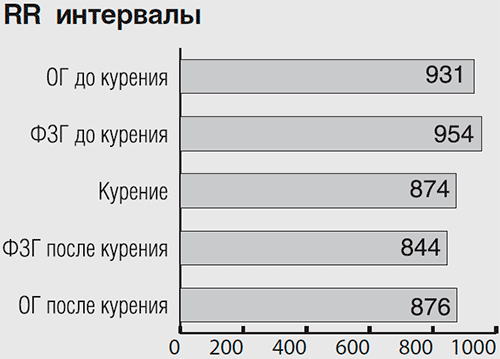
Рисунок 3.4 Значения RR-интервалов частоты сердечных сокращений у испытуемого В.Р. во всех функциональных пробах. Обозначения те же, что и к рисунку 3.1.
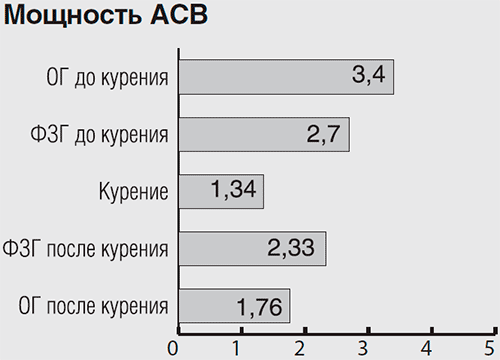
Рисунок 3.5 Значения мощности амплитуды систолической волны (АСВ) у испытуемого В.Р. во всех функциональных пробах. Обозначения те же, что и к рисунку 3.1.
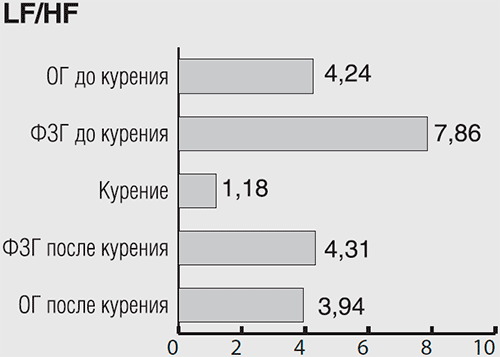
Рисунок 3.6 Значения показателя LF/HF – соотношение низкочастотного (LF) компонента спектра мощности в диапазоне 0,04- 0,15 Гц и высокочастотного (HF) компонента спектра мощности в диапазоне 0,15-0,40 Гц у испытуемого В.Р. во всех функциональных пробах.
Обозначения те же, что и к рисунку 3.1.
Из гистограмм 3.1-3.6 можно заключить, что во время курения:
активность мозга испытуемого В.Р. увеличивается (мощность альфа-ритма уменьшается на 30%, а мощность бета-ритма увеличивается почти на 200%);
активность ВНС претерпевает разнонаправленные изменения с доминированием влияний со стороны симпатического отдела: ЧСС увеличивается на 10%, RR и АСВ уменьшаются на 60% (симпатические компоненты), а отношение LF/HF уменьшается на 70% (парасимпатический компонент).
По данным таблицы 3.4 можно заключить, что во время курения у испытуемых второй группы увеличивается активность как центральной нервной системы мозга (ЭЭГ), так и симпатического отдела ВНС, за исключением двух случаев.
Из 32 значений испытуемых третьей группы двадцать восемь свидетельствуют о том, что во время курения у них увеличивается активность как центральной нервной системы мозга (ЭЭГ), так и симпатического отдела ВНС.
Из данных таблицы 3.4 для четвертой группы следует, что во время курения у испытуемых этой группы увеличивается, за исключением трех случаев, активность как центральной нервной системы мозга (ЭЭГ), так и симпатического отдела ВНС.
Обсуждение результатов
Результаты контрольных групп
Рассмотрим психофизиологические особенности функционального состояния испытуемых одной из контрольных групп (первой) – не курящих во время и после выкуривания своей первой сигареты.
Экспериментальные данные свидетельствуют о разнонаправленных изменениях активности ВНС, мозга и интегральных психологических показателей у испытуемых этой группы. Судя по показателям «САН», курение вызывает у них ухудшение самочувствия, активности и настроения. Физиологи традиционно связывают это с активацией на начальных стадиях курения парасимпатического отдела ВНС, где в качестве нейромедиатора доминирует ацетилхолин (АХ) (Дубынин с соавт., 2010). Однако в нашем случае мы видим, что большая часть физиологических показателей активности ВНС (ЧСС, RR, АСВ) у испытуемых этой группы во время и после курения изменяется по симпатикотропному типу за исключением показателя LF/HF, обнаруживающему заметные индивидуальные вариации (табл. 3.3). Показатели активности мозга (табл. 3.2, гистограммы 3.1-3.6) также обнаруживают разнонаправленные изменения, которые, однако, в целом характеризуются повышением активности (уменьшением мощности альфа-ритма и увеличением мощности бета-ритма).
Практически у всех физиологических показателей (и мозга, и ВНС) во всех ФП наблюдаются в разной степени выраженные эффекты последействия акта курения. При этом, направление (увеличение или уменьшение) показателей совпадает с направлением изменений этих показателей непосредственно при курении. Это согласуется с данными таблицы 3.3, из которой следует, что у большей части испытуемых после курения все физиологические показатели активности ВНС, за исключением АСВ, изменяются по симпатикотропному типу. Такой паттерн изменений показателей активности мозга и ВНС после курения в точности совпадает с паттерном их изменений при курении.
Все вышеизложенное согласуется с общеизвестными эмпирическими данными о функциональных состояниях начинающих курильщиков. Но есть одно исключение – испытуемая К.Е., у которой оценки «САН» резко увеличились в 2-3 раза после выкуривания сигареты. Эта испытуемая отличалась от других членов группы исходно (до эксперимента) низкими самооценками самочувствия и настроения. Это позволяет сформулировать следующие гипотезы, требующие специальной проверки:
повышение оценок «САН» является результатом активного «погружения» К.Е. в роль испытуемой, о чем, в частности, свидетельствует повышение оценки общей активности на 18.2%[1];
никотиновые АХ-рецепторы аналогично мускариновым АХ-рецепторам, норадренэргическим и серотонинэргическим нейронам могут выполнять функции «модуляторов» нервной системы: при наличии исходно низкого (как у испытуемой К.Е.) уровня возбуждения мозга активация никотиновых АХ-рецепторов вызывает повышение уровня бодрствования и наоборот (Дубынин с соавт., 2010).
В целом, разнонаправленные изменения активности мозга и ВНС у некурящих испытуемых во время и после курения можно интерпретировать как своеобразную «разбалансировку» в слаженной работе организма на воздействие непривычного раздражителя.
Теперь обратимся к психофизиологической характеристике функционального состояния членов других контрольных групп – курящих во время эксперимента без контроля над процессом курения.
Это испытуемые 2 и 3 экспериментальных групп. Напомним, что во 2 группу были включены хронические курильщики, которые за весь свой стаж курения не делали перерывов в табакокурении. В третью (контрольную) группу вошли испытуемые, которые регулярно курят табак, но, по условию эксперимента, не курили в течение 24 часов до эксперимента. Из сравнительного анализа данных таблиц 3.1-3.4 следует, что реакции мозга и ВНС испытуемых этих групп мало чем отличались между собой: они характеризовались доминированием процессов возбуждения над процессами торможения: во время курения у испытуемых этих групп увеличивается активность как мозга, так и симпатического отдела ВНС.
Эти показатели хорошо согласуются с общеизвестными данными о динамике нервного возбуждения по мере увеличения стажа курения, заключающейся в постепенной замене «парасимпатикотропного» типа активности на «симпатикотропный». При этом на психологическом уровне обнаруживается четко выраженный эффект привыкания, который, в отличие от показателей 1 группы, выражается в незначительном колебании оценок «САН» после выкуривания всего лишь одной сигареты.
Результаты экспериментальной группы
Напомним, что в экспериментальную (четвертую) группу вошли хронические курильщики, которые в процессе курения сигареты в эксперименте следили за количеством выкуриваемого табака. Контролировать этот процесс помогали нанесенные заранее риски на сигарете (Захаров, 2011).
Рассмотрим психофизиологические особенности функционального состояния этих испытуемых во время и после выкуривания сигареты. Как видно из таблицы 3.1, изменения их самооценок самочувствия, активности и настроения в результате курения с контролем над выкуриваемой дозой табака меняются индивидуально, но в целом (по сумме оценок «САН») с тенденцией к небольшому ухудшению состояния.
Из данных таблицы 3.2 следует, что в целом по группе, мощность бета-ритма во всех ФП увеличивается при разнонаправленном изменении альфа-ритма. Из 32 значений сводной таблицы 3.3 двадцать девять значений показателей ВНС меняются по симпатикотропному типу, свидетельствуя о повышении общего уровня бодрствования испытуемого после выкуривания сигареты. Таким образом, при контроле над процессом курения наблюдается такой же паттерн изменений в активности мозга и ВНС, что и у начинающих курильщиков – дисбаланс активности мозга и ВНС, сопровождаемый нарастанием неприятных самоощущений (уменьшением значений оценок «САН»). Испытуемый на короткое время как бы возвращается в исходное до формирования зависимости от табака состояние «некурящего». Об этом же свидетельствует и сходный характер пространственных кросскорреляций суммарной активности мозга у испытуемых этих групп до и после курения (рисунки 3.7, 3.8).
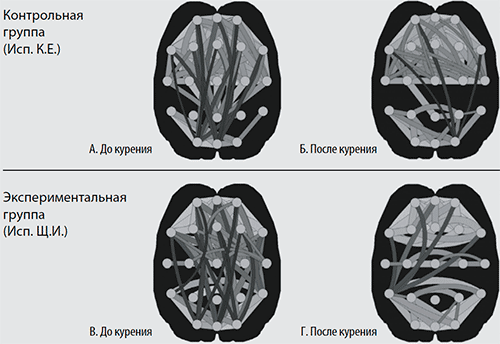
Рисунок 3.7 Обозначения: кружками обозначены места расположения регистрирующих электродов.
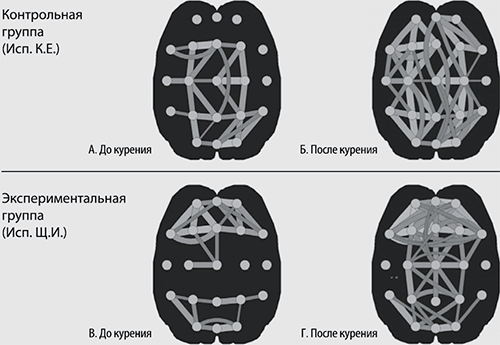
Рисунок 3.8 Обозначения: кружками обозначены места расположения регистрирующих электродов.
Для сравнения на рисунке представлены данные пространственной кросскорреляции активности мозга двух испытуемых в диапазоне альфа-ритма (8-12 Гц; закрытые глаза) до и после курения. Верхние коррелограммы (А, Б) отражают структуру связей между разными участками мозга испытуемого К.Е., никогда не курившего табак и согласившегося выкурить сигарету в эксперименте (контрольная группа 1). Нижние коррелограммы (В, Г) представляют конфигурацию взаимодействующих участков мозга испытуемого Щ.И., курившего сигарету с контролем над количеством выкуриваемого табака (экспериментальная группа).
Для сравнения на рисунке представлены данные пространственной кросскорреляции активности мозга двух испытуемых в диапазоне бета-ритма (13-35 Гц; закрытые глаза) до и после курения. Верхние коррелограммы (А, Б) отражают структуру связей между разными участками мозга испытуемого К.Е., никогда не курившего табак и согласившегося выкурить сигарету в эксперименте (контрольная группа 1). Нижние коррелограммы (В, Г) представляют конфигурацию взаимодействующих участков мозга испытуемого Щ.И., курившего сигарету с контролем над количеством выкуриваемого табака (экспериментальная группа).
Выводы
Функциональные состояния нервной системы и общепсихологического состояния человека во время курения зависят не только от концентрации потребляемого табака и частоты курения, но и от отношения курящего к процессу табакокурения.
Механическое прерывание курения может оказаться менее эффективным средством в борьбе с угрожающим недугом, чем специальным образом (поэтапно) организованная когнитивная активность испытуемого в процессе курения.
Примечания
1.Значение разности: «Оценка А после исследования» минус «Оценка А до исследования», выраженное в процентах к величине «Оценка А до исследования».
Литература:
Баевский Р.М. Медико-физиологические аспекты разработки аппаратно-программных средств для математического анализа ритма сердца / Р.М. Баевский, А.Р. Баевский, М.М. Лапкин, Ю.Н. Семенов, П.В. Шалкин // Российский медико-биологический вестник. – 1996. – № 1-2. – С.104-113.
Гальперин П.Я. Введение в психологию / П.Я. Гальперин. – Москва : Просвещение, 1976.
Гнездицкий В.В. Вызванные потенциалы мозга в клинической практике / В.В. Гнездицкий. – Таганрог, 1997.
Гнездицкий В.В. Обратная задача ЭЭГ и клиническая электроэнцефалография / В.В. Гнездицкий. – Таганрог : ТГРУ, 2000.
Доскин В.А. Тест дифференцированной самооценки функционального состояния / В.А. Доскин, Н.А. Лаврентьева, М.П. Мирошников, В.Б. Шарай // Вопросы психологии. – 1973. – № 6. – С.141-145.
Дубынин В.А. Регуляторные системы организма человека / В.А. Дубынин, А.А. Каменский, М.Р. Сапин, В.И. Сивоглазов. – Москва : Дрофа, 2010.
Захаров С.М. Практическое применение компьютерной электроэнцефалографии / С.М. Захаров, А.М. Скоморохов. – Таганрог : Медиком- МТД, 2012. –[Электронный ресурс]. – Режим доступа : www.medicom-mtd.com
Захаров В.М. Как бросить курить с помощью сигарет / В.М. Захаров. – Воронеж : Изд-во им. Е. А. Болховитинова, 2010. – 93, [1] с. : ил., табл.
Захаров В.М. Сигареты как средство отвыкания от курения / В.М. Захаров // Труды конференции, посвященной 35-летнему юбилею наркологической службы «Лечение и профилактика болезней зависимости». – Воронеж, 2012. – С. 14-16.
Сайт проекта «Никвитин» (NiQuitin) – [Электронный ресурс]. – Режим доступа : https://www.24plan.ru/ – Дата обращения 12.02.2014.
Benowitz N.L. Pharmacology of Nicotine: Addiction, Smoking–Induced Disease, and Therapeutics // Annual Review of Pharmacology and Toxicology. – 2009. – 49. – 57-71.
Fant R.V., Buchhalter A.R., Buchman A.C., Henningfield J.E. Pharmacotherapy for tobacco dependence // Handbook of Experimental Pharmacology. – 2009. – 192. – 487-510.
Galatenko V.V.,
Livshitz E.D., Chernorizov A.M., Zinchenko Yu.P. et al. (2013). Automated
real-time classification of functional states: the significance of individual
tuning stage. Psychology in Russia: State of the Art, 6 (3)
Захаров В.М., Королев А.Д., Черноризов А.М.Новый подход к борьбе с курением: психофизиологический анализ. // Национальный психологический журнал. 2013. № 1. , 91-99. doi: 10.11621/npj.2013.0212
Скопировано в буфер обмена
Скопировать

